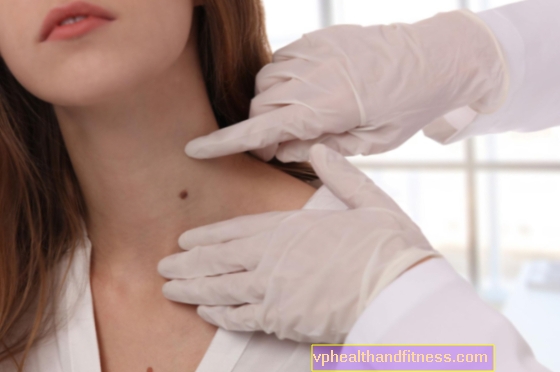
Ống tiêm chứa sẵn liều duy nhất chứa 1,65 mg pegaptanib natri tương ứng với 0,3 mg oligonucleotide axit tự do trong một thể tích danh nghĩa là 90 µl.
| Tên | Nội dung của gói | Hoạt chất | Giá 100% | Sửa đổi lần cuối |
| Macugen | 1 máy tính, giải pháp cho cú sốc | Pegaptanib natri | 2019-04-05 |
Hoạt động
Pegaptanib là một oligonucleotide pegyl hóa được biến đổi liên kết có chọn lọc và mạnh mẽ với dạng ngoại bào của yếu tố tăng trưởng nội mô (VEGF165), ức chế hoạt động của nó. VEGF là một loại protein được tiết ra có tác dụng hình thành mạch, tăng tính thấm thành mạch và chống viêm; tất cả những hành động này dường như giải thích cho sự tiến triển của AMD với sự hình thành mạch. VEGF165 là một dạng đồng dạng VEGF được ưu tiên tham gia vào các khối u mạch máu bệnh lý trong nhãn cầu. Ở những bệnh nhân AMD được điều trị bằng pegaptanib, đã quan sát thấy sự giảm kích thước tổn thương trung bình, kích thước tân mạch màng đệm (CNV) và kích thước rò rỉ fluorescein. Ở động vật, pegaptanib được hấp thu chậm từ mắt vào hệ tuần hoàn sau khi tiêm trong cơ thể. Thời gian bán hủy biểu kiến trung bình ± của pegaptanib trong huyết tương sau khi dùng liều 3 mg cho một mắt (gấp 10 lần liều khuyến cáo) là 10 ± 4 ngày. Nồng độ tối đa trung bình trong huyết tương đạt được từ 1-4 ngày sau khi dùng liều 3 mg vào một mắt. Pegaptanib không tích lũy trong huyết tương sau khi tiêm trong cơ thể mỗi 6 tuần. Pegaptanib được chuyển hóa bởi endo- và exonuclease. Nó được bài tiết ở dạng mẹ và các chất chuyển hóa chủ yếu qua nước tiểu.
Liều lượng
Chế phẩm này nên được sử dụng bởi các bác sĩ nhãn khoa có kinh nghiệm trong việc tiêm thuốc trong da. Chế phẩm nên được thực hiện 6 tuần một lần (9 lần tiêm mỗi năm) vào thể thủy tinh của mắt bị ảnh hưởng. Trước khi sử dụng, kiểm tra để đảm bảo rằng dung dịch không bị vẩn đục hoặc đổi màu. Việc tiêm phải được thực hiện trong điều kiện vô trùng với việc rửa tay và khử trùng phẫu thuật, găng tay vô trùng, màn vô trùng và mỏ vịt mắt, và có thể thực hiện nội soi trong điều kiện vô trùng (nếu cần). Bệnh sử của bệnh nhân nên được đánh giá lại cẩn thận xem có phản ứng quá mẫn trước khi tiêm hay không. Nên tiêm thuốc mê thích hợp và kháng sinh phổ rộng tại chỗ trước khi tiêm. Sau khi sử dụng chế phẩm, một sự gia tăng thoáng qua của nhãn áp đã được quan sát thấy, do đó cần theo dõi sự tưới máu của thần kinh thị giác và nhãn áp. Ngoài ra, bệnh nhân cần được theo dõi cẩn thận về tình trạng xuất huyết dịch kính và viêm nội nhãn trong thời gian 2 tuần sau khi tiêm. Nếu sau 2 lần tiêm liên tiếp, bệnh nhân không đạt được lợi ích điều trị nào (mất ít hơn 15 chữ cái trong bài kiểm tra thị lực) ở lần khám điều trị 12 tuần, nên xem xét việc ngừng hoặc gián đoạn điều trị. Ống tiêm được làm đầy sẵn chứa lượng chế phẩm dư thừa. Không được dùng quá nhiều lượng thuốc. Phần dư thừa nên được loại bỏ trong quá trình chuẩn bị cho quy trình quản lý. Không có khuyến cáo đặc biệt nào liên quan đến việc sử dụng thuốc ở bệnh nhân cao tuổi, suy gan hoặc suy thận vừa hoặc nhẹ.
Chỉ định
Bệnh thoái hóa điểm vàng do tuổi già (AMD) dạng mạch (ướt) ở bệnh nhân người lớn.
Chống chỉ định
Quá mẫn với pegaptanib hoặc bất kỳ tá dược nào. Nhiễm trùng nghi ngờ hoặc đang hoạt động của nhãn cầu hoặc vùng lân cận.
Các biện pháp phòng ngừa
Cũng như các chế phẩm dùng trong mắt khác, có thể xảy ra sự gia tăng thoáng qua nhãn áp. Vì lý do này, việc cung cấp máu cho dây thần kinh thị giác cần được kiểm tra và bất kỳ sự gia tăng nhãn áp nào sau khi tiêm thuốc đều phải được điều chỉnh bằng cách điều trị thích hợp. Xuất huyết ngay lập tức (vào ngày tiêm) hoặc chậm có thể xảy ra sau khi tiêm pegaptanib. Thủ thuật tiêm trong cơ thể có nguy cơ gây viêm nội nhãn. Chưa xác định được tính an toàn và hiệu quả của chế phẩm ở bệnh nhân dưới 18 tuổi. Việc sử dụng nó ở bệnh nhân suy gan hoặc suy thận nặng chưa được nghiên cứu. Việc tiêm toàn bộ thể tích của ống tiêm đã được làm đầy sẵn có thể dẫn đến các tác dụng phụ nghiêm trọng, do đó cần loại bỏ phần dư thừa trước khi tiêm.
Hoạt động không mong muốn
Rất thường gặp: viêm tiền phòng, đau mắt, tăng nhãn áp, viêm giác mạc, kết tủa và đục dịch kính. Thường gặp: nhức đầu, khó chịu ở mắt, đục thủy tinh thể, xuất huyết kết mạc, tăng kết mạc, phù kết mạc, viêm kết mạc, loạn dưỡng giác mạc, khiếm khuyết biểu mô giác mạc, rối loạn biểu mô giác mạc, phù giác mạc, khô mắt, viêm mắt trong, tiết dịch mắt, viêm mắt, kích ứng mắt, ngứa mắt, đỏ mắt, sưng mắt, sưng mí mắt, tăng tiết nước mắt, thoái hóa điểm vàng, giãn đồng tử, khó chịu ở mắt, tăng huyết áp, tụ máu quanh mắt, sợ ánh sáng, nhấp nháy mắt, xuất huyết võng mạc, nhìn mờ, rối loạn thị lực, rối loạn thị giác, bong dịch kính, rối loạn dịch kính, chảy nước mũi.Ít gặp: ác mộng, trầm cảm, nổi hạch, viêm bờ mi, viêm kết mạc dị ứng, lắng đọng giác mạc, xuất huyết mắt, ngứa mí mắt, viêm giác mạc, xuất huyết dịch kính, suy giảm phản xạ đồng tử, mài mòn giác mạc, dịch tiết võng mạc, sụp mí, sẹo võng mạc, màu trắng đục, loét giác mạc, giảm nhãn áp, phản ứng tại chỗ tiêm, phồng rộp chỗ tiêm, bong võng mạc, rối loạn giác mạc, đóng động mạch võng mạc, rách võng mạc, ectropia, chuyển động mắt bất thường, kích ứng mí mắt, xuất huyết buồng trước , Rối loạn đồng tử, rối loạn mống mắt, vàng mắt, viêm màng bồ đào, lắng đọng ở đáy mắt, viêm mống mắt, lúm đồng tiền trong dây thần kinh thị giác, biến dạng đồng tử, tắc tĩnh mạch võng mạc và sa thủy tinh thể, điếc, đợt cấp của bệnh Meniere, chóng mặt, đánh trống ngực bệnh tim, tăng huyết áp, phình động mạch chủ, viêm đau họng, nôn mửa, khó tiêu, viêm da tiếp xúc, chàm, thay đổi màu tóc, phát ban, ngứa, đổ mồ hôi ban đêm, đau lưng, mệt mỏi, ớn lạnh, đau, đau ngực, các triệu chứng giống cúm, tăng mức GGT, mài mòn. Chưa biết: phản ứng phản vệ (bao gồm cả phù mạch). Theo kinh nghiệm sau khi tiếp thị, các trường hợp hiếm gặp về phản ứng phản vệ / phản vệ, bao gồm cả phù mạch, đã được báo cáo ở bệnh nhân trong vòng vài giờ sau khi dùng pegaptanib và các sản phẩm thuốc khác được sử dụng trong quy trình chuẩn bị tiêm. Do không thể loại bỏ thể tích dư thừa của sản phẩm khỏi ống tiêm đã làm đầy trước khi tiêm, các trường hợp nhãn áp tăng nghiêm trọng đòi hỏi phải chọc thủng buồng trước của mắt đã được báo cáo. Một sự gia tăng liên tục, nhẹ nhãn áp cũng được quan sát thấy sau khi dùng nhiều liều thuốc trong mắt trong một nghiên cứu giám sát sau tiếp thị. Khả năng IOP tăng cao là 1,128 lần với mỗi lần tiêm trong cơ thể tiếp theo (p = 0,0003). Không có sự khác biệt có ý nghĩa thống kê về tỷ lệ tăng nhãn áp giữa bệnh nhân có tiền sử tăng nhãn áp hoặc bệnh tăng nhãn áp và bệnh nhân không có tiền sử.
Mang thai và cho con bú
Pegaptanib chưa được nghiên cứu ở phụ nữ có thai. Các nghiên cứu trên động vật là không đủ, nhưng đã cho thấy tác dụng độc hại đối với chức năng sinh sản ở liều cao và tiếp xúc toàn thân. Tiếp xúc toàn thân sau khi dùng thuốc nội nhãn có khả năng rất thấp. Chế phẩm này chỉ nên được sử dụng trong thời kỳ mang thai nếu lợi ích tiềm năng cho người mẹ tương đương với nguy cơ tiềm ẩn cho thai nhi. Người ta không biết liệu chế phẩm có được bài tiết vào sữa hay không - không nên sử dụng chế phẩm trong thời kỳ cho con bú.
Bình luận
Bệnh nhân có thể bị suy giảm thị lực thoáng qua sau khi dùng thuốc trong da; cho đến khi các triệu chứng này được giải quyết, bạn không nên lái xe hoặc sử dụng máy móc. Bảo quản trong tủ lạnh (2-8 độ C); không đóng băng.
Tương tác
Không có nghiên cứu tương tác thuốc nào được thực hiện. Pegaptanib được chuyển hóa bởi nuclease, do đó không có tương tác nào liên quan đến hệ thống cytochrome P450. Hai nghiên cứu ở giai đoạn đầu được thực hiện ở những bệnh nhân chỉ dùng chế phẩm hoặc chế phẩm và liệu pháp quang động học cho thấy không có sự khác biệt rõ ràng về dược động học huyết tương của pegaptanib.
Chế phẩm có chứa chất: Pegaptanib natri
Thuốc được hoàn lại: KHÔNG



.jpg)
















---jaowa-martwica-gowy-koci-udowej.jpg)